產品年度質量回顧分析系統
質量回顧分析系統(QRS)
—— 減少80%產品年度質量回顧分析工作,無須購買傳統專業的統計分析工具
1979年,美國FDA頒布的藥品GMP規定,要求每個公司應建立自己產品質量標準的評估程序,基于一個年度,對GMP所要求的記錄進行回顧,這一要求在cGMP法規21CFR211.80(e)公布并于1979年3月28日生效。
從2010版國內GMP開始,增加了產品年度質量回顧的規定。“應每年對所有生產的藥品按品種進行產品質量回顧分析,以確認工藝穩定可靠,以及原輔料、成品現行質量標準的適用性,及時發現不良趨勢,確定產品及工藝改進的方向。應考慮以往回顧分析的歷史數據,回顧分析應有文件記錄。”
先騰質量回顧分析系統
先騰質量回顧分析系統將全面集成、生產工藝、原輔料、產品質檢、公用系統、穩定性考察等各類數據,內嵌豐富的統計分析方法,自定義配置多種報告模板,一鍵生成產品年度質量回顧分析報告。
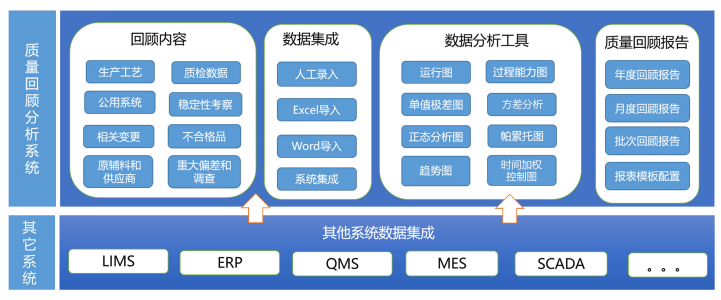
功能介紹
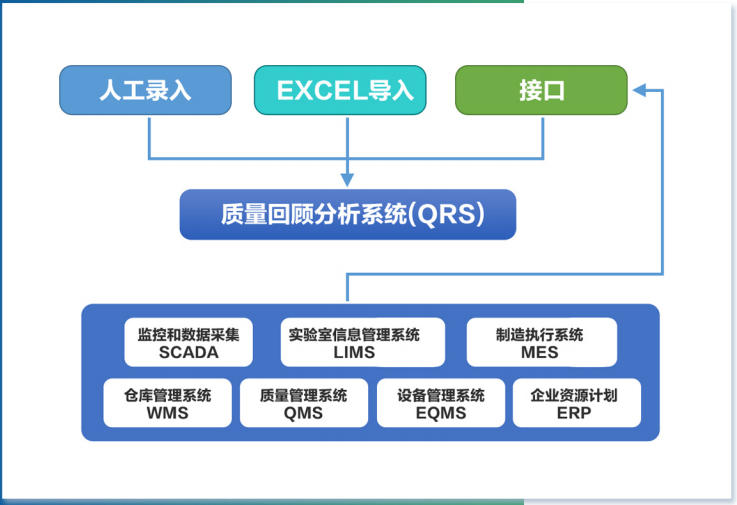
1)數據無縫集成
系統提供人工錄入、Excel導入、接口集成等多種數據采集方式、與ERP、LIMS、MES等系統無縫對接
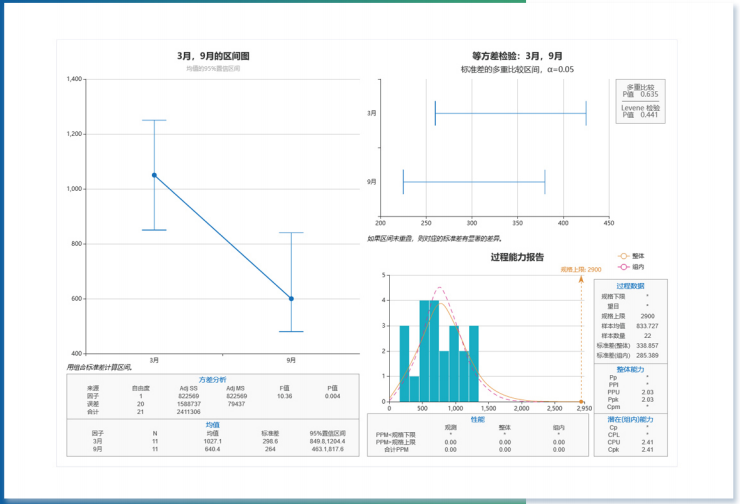
2)數據分析工具
支持趨勢圖、運行圖、單值極差控制圖、過程能力、方差分析、帕累托圖、正態分析圖等常用統計分析方法
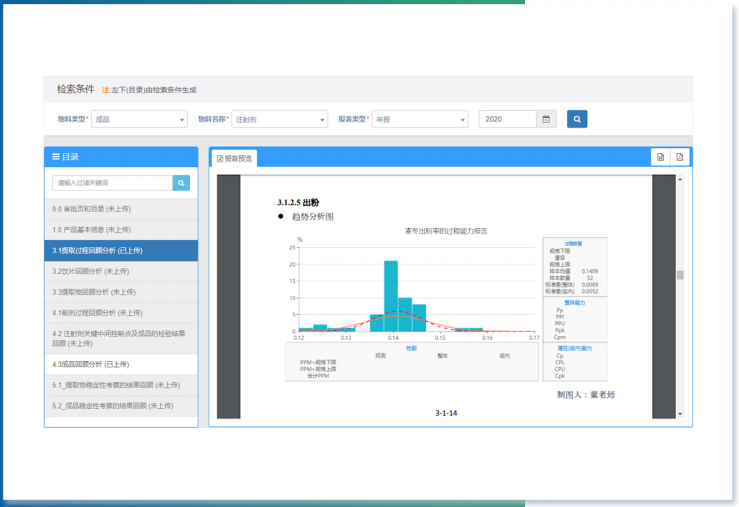
3) 年度報告
用戶可根據企業質量報告模板進行自定義配置,系統支持按照月度、年度等多種方式進行方便快捷的生成、查看、共享產品質量回顧分析報告

詳情介紹
給企業帶來的收益
? 一鍵式生成質量回顧分析報告減少80%質量回顧工作
? 數據共享,消除信息孤島協同辦公,提高辦公效率
? 標準化質量回顧流程和分析模板,提高報告質量
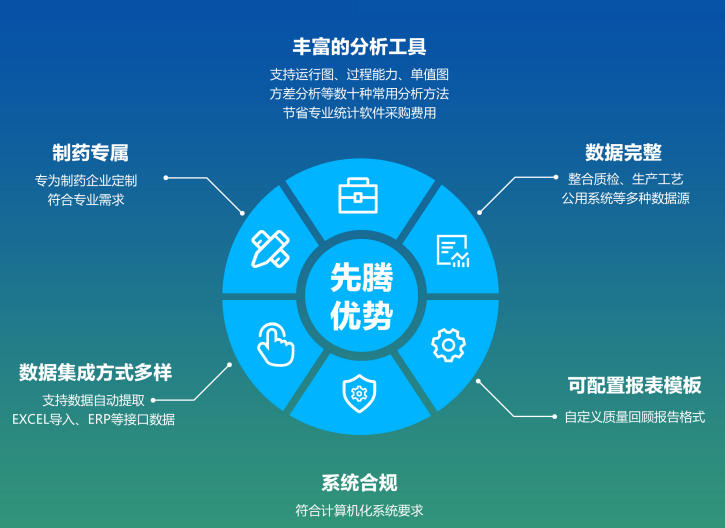
質量回顧分析系統的優勢
1)數據集成方式多樣
? 支持數據自動提取EXCEL導入、ERP等接口數據
2)豐富的分析工具:
? 支持運行圖、過程能力、單值圖
? 方差分析等數十種常用分析方法
? 節省專業統計軟件采購費用
3)可配置報表模板
? 自定義質量回顧報告模式
4)制藥專屬
? 專為制藥企業定制符合專業需求
5)數據完整
? 整合質檢、生產工藝公用系統等多種數據源
6)系統合規
? 符合計算機化系統要求
聯系我們:
北京綠綿科技有限公司
地址:北京市海淀區北四環西路68號左岸工社806室
電話:010-82676061/2/3/45/6/7
傳真:010-82676068
